|
|
95+ Poudre blanche Sorafénib Impureté D CAS 2206827-14-5
|
Détails sur le produit:
Conditions de paiement et expédition:
|
| Nom du produit: | Sorafénib Impureté D | Numéro CAS: | Le numéro de téléphone: |
|---|---|---|---|
| M.W.: | 329.35 | Résultats: | C17H19N3O4 |
| Apparence: | Poudre blanche | La pureté: | 95+ |
| EINECS n°: | - | Réservation: | 5 à 25°C |
Description du produit
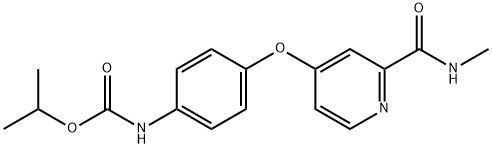
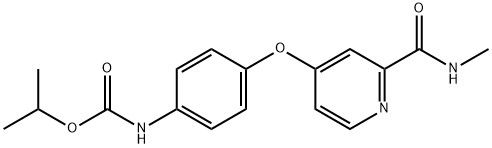
Poudre blanche Sorafénib Impureté D CAS 2206827-14-5 95+
Nom:Impureté du régorafénib D
CAS n°:Le numéro de téléphone:
M.W.- Je ne sais pas.35
Apparence: Poudre blanche
La pureté: Plus de 95 ans
Synonymes:Impureté du régorafénib D
Application du projet
L'impureté D du régorafénib est une impureté spécifique présente dans le régorafénib, un médicament principalement utilisé dans le traitement de certains types de cancer en tant qu'inhibiteur de la multi-kinase.lorsqu' il s' agit de l' application du régorafénib Impureté D, il n' est pas utilisé comme principe actif à des fins thérapeutiques.
En fait, les impuretés dans les médicaments sont des facteurs qui nécessitent un contrôle strict pendant la fabrication pharmaceutique pour assurer la sécurité et l'efficacité du médicament.Des concentrations élevées d'impuretés peuvent affecter la puretéLes résultats de l'analyse de la toxicité et de la stabilité et de l'activité biologique du médicament, entraînant des effets indésirables ou une diminution des bénéfices thérapeutiques.Le contrôle des impuretés est une étape cruciale dans le développement et la production de médicaments..
L'étude du régorafénib Impureté D se concentre sur la compréhension de ses propriétés chimiques, de ses activités biologiques potentielles et des mécanismes de sa formation pendant la production et le stockage du médicament.En menant des recherches approfondies sur cette impureté, les sociétés pharmaceutiques peuvent optimiser leurs processus de fabrication, réduire les niveaux d'impuretés et, en fin de compte, améliorer la qualité et la sécurité du produit final.
Le paquet
![]()
![]()
![]()
![]()
Les transports
Les petits colis ((1g, 25g, 1Kg, 25Kg) peuvent être expédiés par Express. (DHL, FedEx, EMS, etc.)
Les colis de grande taille ((100 kg et plus de100 kg) peuvent être transportés par voie aérienne ou maritime.
Tout le transport est conforme aux besoins du client.
Profil de l'entreprise
![]()
![]()
![]()
![]()
![]()
![]()
Personne à contacter: admin
-
98+ Impuretés de poudre blanche ((Normes) 6-chlor-N-méthylpyridine-2-carboxamide CAS 845306-04-9
-
98+ poudre blanche TICAGRELOR CAS 1129683-88-0 C14H14N4O3
-
98+ Impuretés de la poudre blanche ((Normes) Impureté du sorafénib 16 CAS 2206827-12-3
-
98+ poudre blanche Sorafénib Composé associé 8 NO. 1431697-81-2 CAS
-
98+ Poudre blanche Sorafénib Impureté 6 CAS 1285533-84-7
-
Pure poudre blanche de 98+ Sorafénib Impureté 3 N° CAS 284670-98-0 C27H24N6O5